Obsah
- TL; DR (príliš dlho; neprečítané)
- Klasifikácia propánu
- Chemický vzorec propánu
- Štruktúra propánu
- Vlastnosti propánu
- Použitie propánu
Propán je fosílne palivo a je súčasťou zemného plynu. V priebehu miliónov rokov sa tvoril z organických zvyškov organizmov a ťažil sa z podzemných ložísk. Propánový plyn je organická zlúčenina vyrobená z troch molekúl atómov uhlíka spojených s ôsmimi atómami vodíka. Druh väzieb uhlík - uhlík - vodík určuje štruktúru molekúl propánu, ktorá má rovnaký vzorec ako ostatné typy prírodných plynov, ako je metán a bután.
TL; DR (príliš dlho; neprečítané)
TL; DR (príliš dlho; neprečítané)
Chemický vzorec propánu je C3H8.
Klasifikácia propánu
Propán je klasifikovaný ako organická zlúčenina, pretože obsahuje uhlík. Ďalej sa klasifikuje ako uhľovodík, pretože patrí do skupiny organických zlúčenín, ktoré sú vyrobené iba z uhlíka a vodíka. Presnejšie povedané, propán je druh uhľovodíka nazývaný alkán. Atómy v alkánových molekulách sú držané pohromade jednoduchými kovalentnými väzbami a atómy uhlíka vždy tvoria štyri kovalentné väzby.
Chemický vzorec propánu
Alkány majú všeobecný vzorec so stanoveným pomerom atómov uhlíka k atómom vodíka: C_nH2_n+2, Najjednoduchším alkánom je metán, inak známy ako zemný plyn. Obsahuje jeden atóm uhlíka viazaný na štyri atómy vodíka. Pre metán n = 1, takže počet atómov vodíka, ktorý má, sa rovná 2 (1) +2, čo sa rovná 4. Etán obsahuje dva atómy uhlíka viazané spolu, a každý uhlík je viazaný k trom atómom vodíka pre celkom šesť atómov vodíka. Propán má reťazec troch atómov uhlíka s chemickým vzorcom C3H8, pretože reťazec troch uhlíkov vyžaduje 2 (3) +2 atómy vodíka, čo sa rovná ôsmim. Bután, ďalší bežný alkán používaný ako palivo v ručných plynových horákoch, má štyri atómy uhlíka spojené s desiatimi atómami vodíka, s chemickým vzorcom C4H10.
Štruktúra propánu
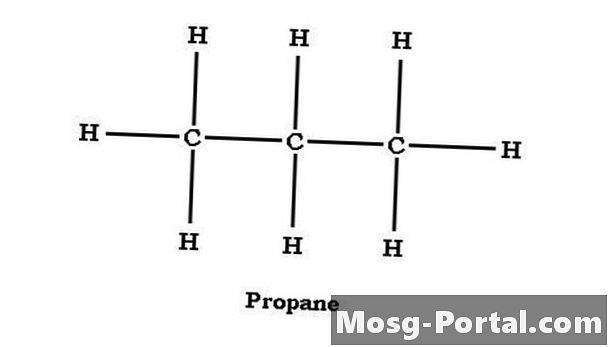
Alkány môžu byť štruktúrované ako priame alebo rozvetvené reťazce. Propán je alkán s priamym reťazcom so štruktúrnymi atómami uhlíka C-C-C. Stredný uhlík zdieľa jednu väzbu s každým z koncových atómov uhlíka a má dva atómy vodíka. Každý z koncových atómov uhlíka má spoločnú väzbu s centrálnym atómom uhlíka a každý je viazaný s tromi atómami vodíka. Pokiaľ ide o jednotlivé atómy uhlíka, propán sa môže vyjadriť ako CH3CH2CH3, čo je ekvivalent k C.3H8 ale robí propánovú štruktúru jasnejšou.
Vlastnosti propánu
Okrem štruktúrnych podobností zdieľaných alkánmi s priamym reťazcom majú rovnaké vlastnosti. Propán a iné uhľovodíky sú nepolárne. Táto vlastnosť vyžaduje, aby sa mohli zmiešať iba s inými nepolárnymi látkami. Napríklad oleje a iné palivá sa vyrábajú zo zmesi uhľovodíkov. Nebudú sa miešať s polárnymi látkami, ako je voda; príťažlivosť medzi molekulami oddeľuje olej a vodu. Pri alkánoch s priamym reťazcom sa teplota varu a teplota topenia zvyšujú so zvyšujúcim sa počtom uhlíkových molekúl. Bod varu propánu je - 44 stupňov Fahrenheita (- 42 stupňov Celzia) a teplota topenia - 306 stupňov Fahrenheita (- 189 stupňov Celzia). Metán s iba jedným uhlíkom má nižšiu teplotu varu ako propán pri -164 stupňov Celzia. Oktán má osem atómov uhlíka a bod varu 98 stupňov Celzia.
Použitie propánu
Vďaka svojmu nízkemu bodu varu sa obvykle nachádza propán v plynnom stave. Keď sa na propán aplikuje správne množstvo tlaku a teploty, prechádza procesom nazývaným skvapalňovanie, ktorý tlačí propánový plyn do jeho kvapalného stavu. Propán sa môže skladovať ako kvapalina v tlakových nádržiach vysoko nad bodom varu. Skvapalnený propánový plyn sa používa ako vykurovacie palivo, ktoré sa spaľuje do energetických pecí a ohrievačov teplej vody. Používa sa tiež ako palivo na varenie pre vonkajšie plynové grily a plynové kempingové kachle na varenie. Propanový plyn je tiež súčasťou hnacích plynov používaných v aerosólových plechovkách. Propán sa tiež používa ako zložka v niektorých druhoch lepidiel, tmelov a farieb.