Obsah
Atómy sú najmenšie častice, ktoré si stále zachovávajú chemické vlastnosti prvku. Skladajú sa zo subatomárnych častíc nazývaných neutróny, elektróny a protóny. Ióny sú nabité atómy alebo skupiny atómov. Ióny môžu byť nabité pozitívne alebo negatívne. Pozitívne nabité ióny sa nazývajú katióny. Záporne nabité ióny sa nazývajú anióny.
Atómy tvoria prvky založené na počte protónov, ktoré majú. Iónové náboje sa prideľujú na základe počtu elektrónov, ktoré má ión.
Atóm
Prvky sú základné látky, vyrobené z atómov, ktoré sa nedajú ďalej chemicky meniť alebo rozkladať. Atómy pozostávajú z jadra jadra a orbitálnych elektrónov. Jadro je tvorené protónmi a neutrónmi. Protóny sú malé častice, ktoré majú mierne kladný náboj. Neutróny majú približne rovnakú veľkosť ako protóny. Nemajú žiadne poplatky. Elektróny sú veľmi malé, dokonca menšie ako protóny a neutróny. Elektróny majú mierne záporný náboj. Počet protónov v jadre atómu určuje, ktorý prvok atóm tvorí. Počet elektrónov, najmä valenčných elektrónov, obiehajúcich okolo jadra, určuje, ako reaktívny je atóm.
Valenčné elektróny
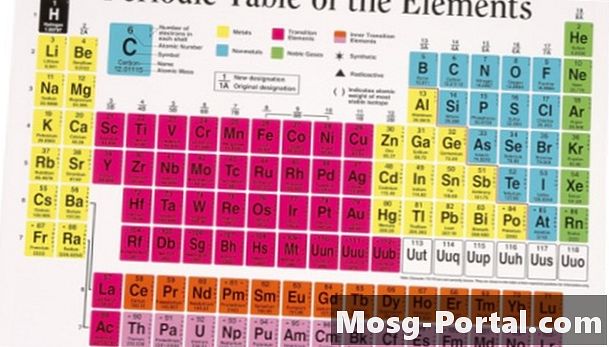
Elektróny obiehajú okolo atómového jadra, pretože sú priťahované k pozitívne nabitým protónom. Nedrží sa jadra, pretože sú odrazené zápornými nábojmi ostatných elektrónov. Elektróny majú tendenciu obiehať vo vrstvách nazývaných mušle. Každý obal je „naplnený“, keď obsahuje oktet s ôsmimi elektrónmi. Vonkajší obal obsahuje valenčné elektróny. Valenčné elektróny určujú, ako reaktívny je prvok. Atómy rôznych prvkov majú rôzne počty elektrónov. Počet valenčných elektrónov, ktoré mal atóm, je možné určiť pomocou periodickej tabuľky. V periodickej tabuľke je osem stĺpcov a prvky sú usporiadané do jedného z ôsmich stĺpcov. Počet valenčných elektrónov v prvku zodpovedá jeho stĺpcu v rozmedzí od jedného do ôsmich. Ušľachtilé plyny v 8. stĺpci majú oktet valenčných elektrónov a nie sú príliš reaktívne.
Úplné oktety
Ušľachtilé plyny sú veľmi stabilné, pretože majú plný vonkajší obal. Väčšina prvkov, s výnimkou ťažkých kovov, lantanoidov a aktinidov, sa riadi oktetovým pravidlom. Pravidlo oktetu uvádza, že prvky majú tendenciu podstúpiť reakcie, ktoré vedú k úplnému valenčnému obalu. Atómy s úplnými vonkajšími škrupinami nie sú príliš reaktívne, pretože sú energeticky stabilné. Atómy vymieňajú elektróny na zvýšenie stability.
Elektrónový prenos
Ióny sa tvoria, keď atómy prenášajú elektróny. Všetky atómy „chcú“ mať vo svojich vonkajších škrupinách celú oktetovú elektrónu. Atómy so siedmimi valenčnými elektrónmi budú chcieť získať jeden elektrón tak, aby mal celkom osem. Získanie jedného je jednoduchšie, ako stratiť sedem. Atómy s jedným valenčným elektrónom chcú prísť o elektrón, ktorý klesne na plný náboj. Strata jedného je jednoduchšia ako získanie siedmich. Elektróny majú záporný náboj, takže atómy, ktoré získavajú elektrón na dokončenie oktetu, získavajú aj záporný náboj a stávajú sa aniónmi. Atómy, ktoré stratia elektrón, strácajú negatívny náboj a stávajú sa katiónmi. Atómy, ktoré stratia alebo získajú viac elektrónov, strácajú alebo získavajú viacnásobné náboje.